女性福音,干細胞在乳腺癌治療領域又有新進展!
由于性別差異、男女內分泌水平差異、激素分泌種類、生活方式等差別因素,很多惡性疾病,會呈現出以性別區分的特點。像是痛風、前列腺癌、肺癌通常男性多發,而甲狀腺癌、乳腺癌以等則多發于女性。
作為女性高發癌癥,乳腺癌常被稱為“粉紅殺手”,其發病率居于女性惡性腫瘤的首位。隨著定期篩查,以及醫療水平的提高,乳腺癌致死率已經大大下降,但手術依然是患者的首選治療方案,而這也意味著患者治愈癌癥的同時,還需要接受乳房完全或者部分切除術后體貌外觀出現變化的心理影響。
乳房作為女性主要性征器官,進行切除后,會極大地損傷女性的心理健康。基于此因素,尋找一種能夠在不損及肉體的前提下治療乳腺癌的方式,是患者和醫生共同期望的。
腫瘤是怎么發生的呢?傳統理論認為,每個正常人體中都存在癌基因,經過千百年進化保持靜止不增殖狀態。當人體受到外界環境有害因素刺激后,如病毒和毒物等,使體內專門調控細胞繁殖速度的基因失控,導致細胞瘋狂擴增而形成腫瘤。
對癌癥致病原理有了解的人會知道,“土壤”、“種子”理論是癌癥干細胞的基礎理論。作為癌變組織擴散和增值的基礎,癌癥干細胞是腫瘤細胞中的一種能夠進行自我補充的細胞,它們能夠使癌癥進一步惡化,甚至讓被治愈的癌癥在一段時期后復發。
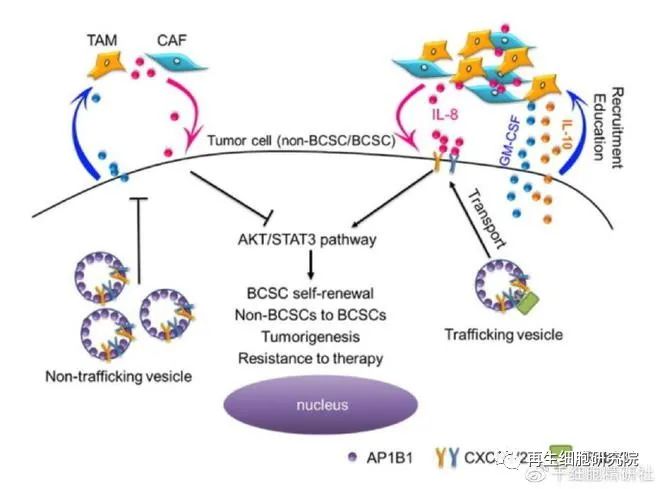
圖.Rab13控制微環境細胞
圖.Rab13控制微環境細胞
近期,中國科學院昆明動物研究所焦保衛團隊助理研究員王慧在Cancer Research上,在線發表了題為Rab13 sustains breast cancer stem cells by supporting tumor-stroma crosstalk的研究論文。
論文內容主要是確認到小GTP酶-Rab13在乳腺癌干細胞中的調控作用:Rab13缺失抑制兩類受體(CXCR1/2)的運輸,使其不能定位于細胞膜上,因此不能響應微環境中IL-8的刺激,進而打斷腫瘤和微環境細胞的“互作”,干擾微環境細胞的可塑性。這些分子化學反應機制,決定了乳腺癌干細胞干性、乳腺癌發生、耐藥性、乳腺癌復發,以及乳腺癌干細胞和非乳腺癌干細胞之間的轉變。
研究人員進一步從FDA老藥中篩選,鑒定到靶向Rab13的化合物-甲基多巴索隆(bardoxolone-methyl, CDDO-Me)。在小鼠移植瘤模型和轉基因成瘤模型中,該腎科藥物處理均能顯著打斷乳腺癌細胞與微環境細胞的“互作”,降低乳腺癌干細胞干性。該研究鑒定了打斷腫瘤干細胞與其微環境“互作”的關鍵機制,針對該機制鑒定到成藥性較好的化合物,將為靶向乳腺癌干細胞提供新策略。
除了提供靶向乳腺癌干細胞的方向,干細胞之所以可以針對乳腺癌,還因為其能分泌抑制因子,作為干細胞用于抑制癌細胞生長的一種方式,該方法同樣也適用于對乳腺癌細胞生長進行抑制。常被使用的干細胞歸巢功能,在癌癥治療中也有出現,其會移動到炎癥和癌細胞增生部位,產生抑制因子,并分化增殖為多種免疫細胞,為人體免疫系統增添一份力量。
對于乳腺癌的治療一直是醫學界亙古不變的研究課題,臨床治療卻仍然面臨現實困境,因此對于女性來說,定期的篩查是預防乳腺癌最佳的方法。

